
- مؤلف Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:33.
- آخر تعديل 2025-01-22 16:55.
الطاقة التي تفاعل يمكن أن تنتج تستخدم لتسخين المياه أو طهي الطعام أو توليد الكهرباء أو حتى تشغيل المركبات. منتجات تفاعلات الاحتراق هي مركبات أكسجين تسمى أكاسيد.
بجانب هذا ، ما هو مثال واقعي لتفاعل الاحتراق؟
يعد حرق الأخشاب في النار مثالاً على تفاعل الاحتراق. في تفاعل الاحتراق ، تتحد الكربوهيدرات الموجودة في الخشب مع الأكسجين لتتشكل ماء وثاني أكسيد الكربون. هذا التفاعل نشيط للغاية ، ويولد الحرارة والضوء أثناء إطلاقه لتلك الطاقة.
علاوة على ذلك ، ما هي بعض الأمثلة على الاحتراق؟ أمثلة على تفاعلات الاحتراق
- احتراق الميثان. CH4(ز) + 2 س2(ز) → CO2(ز) + 2 ح2يا (ز)
- حرق النفثالين.
- احتراق الإيثان.
- احتراق البيوتان (شائع في الولاعات)
- احتراق الميثانول (المعروف أيضًا باسم كحول الخشب)
- احتراق البروبان (المستخدم في شوايات الغاز والمدافئ وبعض مواقد الطهي)
بهذه الطريقة ، ما أهمية تفاعل الاحتراق؟
تفاعلات الاحتراق للغاية الأهمية فئة من المواد الكيميائية تفاعلات . هؤلاء تفاعلات حيوية في حياتنا اليومية. أ تفاعل الاحتراق يحدث عندما يكون الوقود والأكسجين تتفاعل ، لإنتاج الحرارة أو الحرارة والضوء. أخرى يمكن التعرف عليها تفاعلات الاحتراق تشمل شمعة مشتعلة أو نار المخيم اللطيفة.
ما هي بعض الأمثلة على تفاعل الاحتراق؟
تفاعلات الاحتراق تحدث عندما يتفاعل الأكسجين مع مادة أخرى وينتج عنه حرارة وضوء. حرق الفحم وغاز الميثان والمشرقات كلها شائعة أمثلة من تفاعلات الاحتراق . في الأساس ، أي تفاعل الذي يتضمن حرق شيء ما هو ملف تفاعل الاحتراق.
موصى به:
هل تفاعل الاحتراق طارد للحرارة أم ماص للحرارة؟

الاحتراق هو تفاعل أكسدة ينتج حرارة ، وبالتالي فهو دائمًا طارد للحرارة. تكسر جميع التفاعلات الكيميائية الروابط أولاً ثم تصنع روابط جديدة لتشكيل مواد جديدة. كسر الروابط يأخذ الطاقة بينما صنع روابط جديدة يطلق الطاقة
لماذا يعتبر الاحتراق الكامل أفضل من الاحتراق غير الكامل؟

يحدث الاحتراق غير الكامل عندما يكون الإمداد بالهواء أو الأكسجين ضعيفًا. لا يزال يتم إنتاج الماء ، ولكن يتم إنتاج أول أكسيد الكربون والكربون بدلاً من ثاني أكسيد الكربون. يتم إطلاق الكربون كسخام. أول أكسيد الكربون هو غاز سام ، وهذا هو سبب تفضيل الاحتراق الكامل على الاحتراق غير الكامل
كيف يمكن استخدام تفاعل التعادل لإيجاد تركيز القاعدة الحمضية؟

المعايرة هي تجربة يتم فيها استخدام تفاعل معادل للقاعدة الحمضية الخاضعة للرقابة لتحديد التركيز غير المعروف لحمض أو قاعدة. يتم الوصول إلى نقطة التكافؤ عندما يكون عدد أيونات الهيدروجين مساويًا لعدد أيونات الهيدروكسيد
متى يجب استخدام الارتباط ومتى يجب استخدام الانحدار الخطي البسيط؟
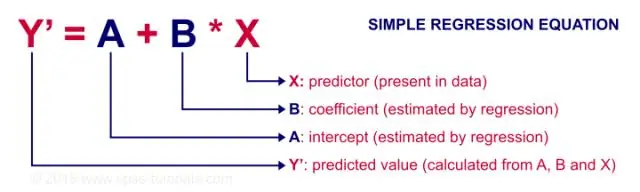
يستخدم الانحدار بشكل أساسي لبناء نماذج / معادلات للتنبؤ بالاستجابة الرئيسية ، Y ، من مجموعة من متغيرات التوقع (X). يستخدم الارتباط بشكل أساسي لتلخيص اتجاه وقوة العلاقات بين مجموعة من 2 أو أكثر من المتغيرات الرقمية بسرعة ودقة
لماذا يتم استخدام ثيوسلفات الصوديوم في تفاعل ساعة اليود؟

يستخدم تفاعل الساعة هذا الصوديوم أو البوتاسيوم أو بيرسلفات الأمونيوم لأكسدة أيونات اليود إلى اليود. يستخدم ثيوسلفات الصوديوم لتقليل اليود مرة أخرى إلى اليود قبل أن يتراكم اليود مع النشا لتشكيل اللون الأزرق والأسود المميز
