
- مؤلف Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:33.
- آخر تعديل 2025-01-22 16:55.
قانون الغاز المثالي ، كما يقول المثل ، هو في الواقع PV = nRT ، مع جميع المتغيرات القياسية. هنا n = m / M ، حيث m هي كتلة الغاز و M هي الوزن الجزيئي للغاز. باختصار فإن R in PV = nRT يتم تصغيره بواسطة عامل M (الوزن الجزيئي) للحصول على R في PV = mRT.
ببساطة ، ما هو r يساوي في pV nRT؟
قانون الغاز المثالي هو: الكهروضوئية = nRT ، حيث n هو عدد الشامات ، و ص هو ثابت غاز عالمي. قيمة ال ص يعتمد على الوحدات المعنية ، ولكن عادة ما يتم ذكرها بوحدات S. I. على النحو التالي: ص = 8.314 جول / مول. هذا يعني أنه بالنسبة للهواء ، يمكنك استخدام القيمة ص = 287 جول / كجم.
وبالمثل ، ما الذي يرمز إليه R في الكيمياء pV nRT؟ وحدات ثابت الغاز العالمي ص مشتق من المعادلة PV = n ص تي. هو - هي مواقف ريجنولت.
في هذا الصدد ، ما الذي ترمز إليه N في pV nRT؟
. قانون فيزيائي يصف العلاقة بين الخصائص القابلة للقياس للغاز المثالي ، حيث P (الضغط) × V (الحجم) = (عدد المولات) × R (الجاسكونستانت) × T (درجة الحرارة بالكلفن). مشتق من مجموعة قوانين الغاز لبويل وتشارلز وأفوجادرو. يسمى أيضا قانون الغاز العالمي.
ما هو M في قانون الغاز المثالي؟
الأصلي قانون الغاز المثالي يستخدم الصيغة PV = nRT ، إصدار الكثافة من قانون الغاز المثالي هو PM = dRT ، حيث P هو الضغط المقاس في الأجواء (atm) ، T هو درجة الحرارة تقاس بالكلفن (K) ، R هي قانون الغاز المثالي ثابت 0.0821 في م (ل) م ol (K) تمامًا كما في الصيغة الأصلية ، ولكن م هي الآن الكتلة المولية (g م رأ
موصى به:
ما هو الفرق بين انتشار التناضح والانتشار الميسر؟

يحدث التناضح أيضًا عندما ينتقل الماء من خلية إلى أخرى. من ناحية أخرى ، يحدث الانتشار الميسر عندما يكون الوسط المحيط بالخلية في تركيز عالٍ من الأيونات أو الجزيئات عن البيئة داخل الخلية. تنتقل الجزيئات من الوسط المحيط إلى الخلية بسبب تدرج الانتشار
ما هو الفرق بين الارتباط ومربع تشي؟
إذن ، الارتباط يدور حول العلاقة الخطية بين متغيرين. عادةً ما يكون كلاهما مستمرين (أو تقريبًا) ولكن هناك اختلافات في الحالة التي يكون فيها أحدهما ثنائي التفرع. عادة ما يتعلق مربع كاي باستقلال متغيرين. عادة ، كلاهما قاطع
ما هو الفرق بين المنطقة المناخية والمنطقة الأحيائية؟

يتم تصنيف المناخ على أساس درجة حرارة الغلاف الجوي وهطول الأمطار بينما يتم تصنيف المنطقة الأحيائية في المقام الأول على أساس أنواع موحدة من الغطاء النباتي. يمكن للمناخ تحديد المنطقة الأحيائية الموجودة ، لكن المنطقة الأحيائية لا تتحكم في المناخ أو تؤثر عليه بنفس الطريقة
ما الفرق بين الإضاءة الصلبة والناعمة؟

الفرق بين الضوء الخافت والضوء الصلب. يصنع الضوء الشديد ظلالًا مميزة ذات حواف صلبة. الضوء الخافت يجعل الظلال غير مرئية بالكاد. يوم مشمس ضوء قاس
ما هو الفرق بين الكيمياء العامة والكيمياء العضوية؟
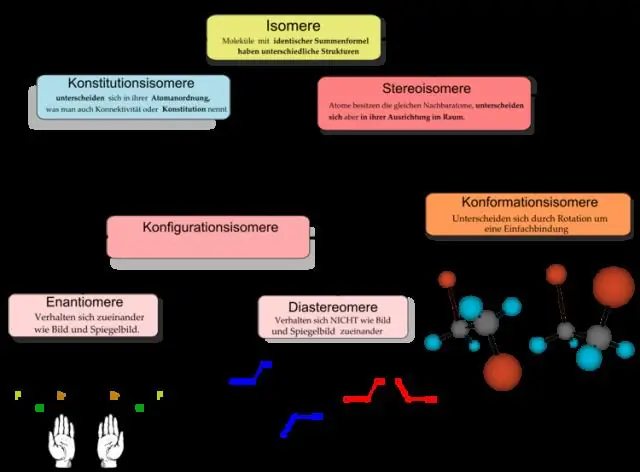
تعتبر الكيمياء العضوية فرعًا فرعيًا للكيمياء. في حين أن المصطلح الشامل "الكيمياء" يهتم بتكوين وتحولات جميع المواد بشكل عام ، فإن الكيمياء العضوية تقتصر على دراسة المركبات العضوية فقط
