- مؤلف Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:33.
- آخر تعديل 2025-01-22 16:55.
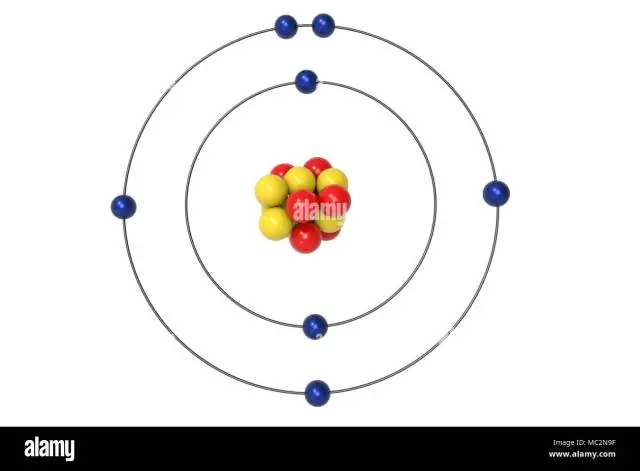
ستذهب الإلكترونات الثلاثة المتبقية في المدار 2p. لذلك سيكون تكوين الإلكترون N هو 1 ثانية22 ثانية22 ص3. التكوين الرموز يوفر النيتروجين (N) طريقة سهلة للعلماء لكتابة وتوصيل كيفية ترتيب الإلكترونات حول نواة ذرة النيتروجين.
هنا ، ما هو تكوين إلكترون التكافؤ لذرة النيتروجين؟
[هو] 2s2 2p3
قد يتساءل المرء أيضًا ، لماذا تكافؤ النيتروجين هو 5؟ نتروجين تم العثور على إما 3 أو 5 التكافؤ الإلكترونات وتقع في قمة المجموعة 15 على الجدول الدوري. يمكن أن تحتوي على 3 أو 5 التكافؤ الإلكترونات لأنها يمكن أن تترابط في المدارات الخارجية 2p و 2s. نتروجين يشكل الحمض النووي في شكل قواعد نيتروجينية وكذلك في الناقلات العصبية.
بعد ذلك ، السؤال هو ، ما هو تكوين إلكترون التكافؤ الأساسي للبوتاسيوم؟
هكذا، البوتاسيوم لديه التوزيع الإلكترون من [ar] 4s1. بالتالي، البوتاسيوم يتوافق مع Li و Na في ملفه تكوين قذيفة التكافؤ . التالي إلكترون يضاف لإكمال 4s subshell والكالسيوم له التوزيع الإلكترون من [ar] 4s2.
كيف تحدد التكافؤ؟
ال تكافؤ من الذرة يساوي عدد الإلكترونات في الغلاف الخارجي إذا كان هذا الرقم أربعة أو أقل. وإلا فإن تكافؤ يساوي ثمانية ناقص عدد الإلكترونات في الغلاف الخارجي. بمجرد معرفة عدد الإلكترونات ، يمكنك ذلك بسهولة احسب ال تكافؤ.
موصى به:
كيف تصحح أخطاء إلكترون؟

الإلكترون - التصحيح. لدينا عمليتان تقومان بتشغيل تطبيقنا - العملية الرئيسية وعملية العارض. نظرًا لأن عملية العارض هي العملية التي يتم تنفيذها في نافذة المتصفح ، يمكننا استخدام Chrome Devtools لتصحيحها. لفتح DevTools ، استخدم الاختصار "Ctrl + Shift + I" أو المفتاح
ما الذي يعتبر مجموعة إلكترون واحدة؟

يمكن أن تكون مجموعة الإلكترون عبارة عن زوج من الإلكترونات ، أو زوجًا منفردًا ، أو إلكترونًا منفردًا ، أو رابطة مزدوجة أو رابطة ثلاثية على الذرة المركزية. باستخدام نظرية VSEPR ، ستساعدنا أزواج الرابطة الإلكترونية والأزواج المنفردة في الذرة المركزية على التنبؤ بشكل الجزيء
ما هي الشحنة الرسمية للنيتروجين في هذا الهيكل؟

بالاستمرار مع النيتروجين ، نلاحظ أنه في (أ) تشترك ذرة النيتروجين في ثلاثة أزواج من الترابط ولها زوج وحيد ولديها إجمالي 5 إلكترونات تكافؤ. وبالتالي ، فإن الشحنة الرسمية على ذرة النيتروجين هي 5 - (2 + 6/2) = 0. في (ب) ، تحتوي ذرة النيتروجين على شحنة رسمية قدرها -1
ما هو تكوين إلكترون الحالة الأرضية لذرة الفضة؟

تكوين إلكترون الحالة الأرضية للفضة المحايدة الغازية الحالة الأرضية هو [Kr]. 4d10. 5s1 ورمز المصطلح هو 2S1 / 2
ما هي طاقة التأين kJ mol للنيتروجين؟

طاقة التأين للنيتروجين الجزيئي هي 1503 كيلو جول مول -1 ، وطاقة النيتروجين الذري 1402 كيلو جول مول -1. مرة أخرى ، تكون طاقة الإلكترونات في النيتروجين الجزيئي أقل من طاقة الإلكترونات في الذرات المنفصلة ، لذلك يرتبط الجزيء
