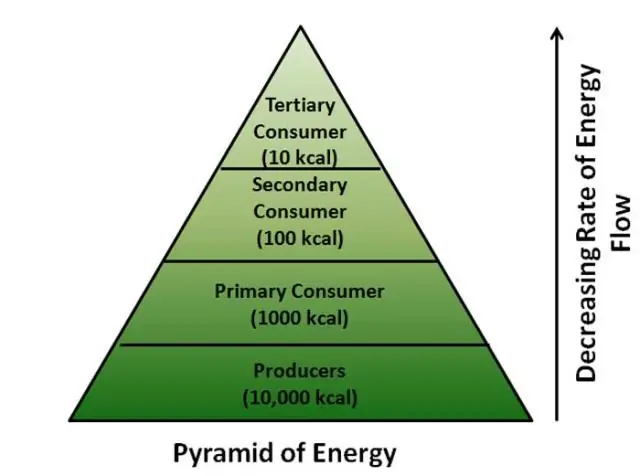
الهرم البيئي (أيضًا هرم غذائي ، هرم إلتوني ، هرم طاقة ، أو هرم غذائي في بعض الأحيان) هو تمثيل رسومي مصمم لإظهار الكتلة الحيوية أو الإنتاجية الحيوية في كل مستوى غذائي في نظام بيئي معين
في حالة حدوث تفاعل ماص للحرارة ، تكون المواد المتفاعلة عند مستوى طاقة أقل مقارنة بالمنتجات - كما هو موضح في مخطط الطاقة أدناه. في حالة حدوث تفاعل طارد للحرارة ، تكون المواد المتفاعلة عند مستوى طاقة أعلى مقارنة بالمنتجات ، كما هو موضح أدناه في مخطط الطاقة
لتجميع شجرتين أو أكثر ، أو لزرع صف تحوط ، اترك مسافة لا تقل عن 15 إلى 20 قدمًا بين تنوب دوغلاس الصغير. ضع كل شجرة في حفرة بعمق 2 قدم وعرض 3 أقدام ، وقم بفك الجذور ونشرها قبل ردمها بالأوساخ
يشمل الطيف الكهرومغناطيسي بأكمله ، من أدنى تردد إلى أعلى تردد (من أطول إلى أقصر طول موجي) ، جميع موجات الراديو (على سبيل المثال ، الراديو والتلفزيون التجاريين ، الموجات الدقيقة ، الرادار) ، الأشعة تحت الحمراء ، الضوء المرئي ، الأشعة فوق البنفسجية ، الأشعة السينية ، و أشعة غاما
حساب الانحراف المعياري حساب متوسط العملية μ اطرح متوسط العملية من كل قيمة بيانات مُقاسة (قيم X i) قم بتربيع كل الانحرافات المحسوبة في الخطوة 2. اجمع كل الانحرافات التربيعية المحسوبة في الخطوة 3. اقسم نتيجة الخطوة 4 بحجم العينة
يعد الالتفاف الفائق للحمض النووي مهمًا لتعبئة الحمض النووي داخل جميع الخلايا. نظرًا لأن طول الحمض النووي يمكن أن يكون آلاف المرات من الخلية ، فإن تغليف هذه المادة الجينية في الخلية أو النواة (في حقيقيات النوى) يعد إنجازًا صعبًا. يقلل اللف المفرط للحمض النووي من المساحة ويسمح بتعبئة الحمض النووي
تشمل النباتات الوعائية الخالية من البذور السرخس وذيل الحصان والطحالب. هذه الأنواع من النباتات لها نفس الأنسجة الخاصة لنقل الماء والغذاء من خلال سيقانها وأوراقها ، مثل النباتات الوعائية الأخرى ، لكنها لا تنتج الزهور أو البذور. بدلاً من البذور ، تتكاثر النباتات الوعائية الخالية من البذور مع الأبواغ
نظرًا للكم الهائل من الطاقة اللازمة لإطلاق طائرة نفاثة نسبية ، فمن المحتمل أن تعمل بعض الطائرات عن طريق تدوير الثقوب السوداء. تشرح هذه النظرية استخراج الطاقة من الحقول المغناطيسية حول قرص التراكم ، والذي يتم جره ولفه بواسطة دوران الثقب الأسود
دورة الخلية عبارة عن سلسلة من الأحداث التي تحدث في الخلية أثناء نموها وانقسامها. تقضي الخلية معظم وقتها فيما يسمى الطور البيني ، وخلال هذا الوقت تنمو وتكرر كروموسوماتها وتستعد لانقسام الخلية. ثم تغادر الخلية الطور البيني ، وتخضع للانقسام ، وتكمل انقسامها
في نظام تصنيف محتوى السيليكا المقبول على نطاق واسع ، تسمى الصخور التي تحتوي على أكثر من 65 في المائة من السيليكا بالفلسيك ؛ أولئك الذين تتراوح أعمارهم بين 55 و 65 في المائة من السيليكا هم من الوسط ؛ أولئك الذين لديهم ما بين 45 و 55 في المائة من السيليكا هم مافيك ؛ وأولئك الذين لديهم أقل من 45 في المائة هم فوق ماف